¿Cuáles son los criterios para clasificar materiales?
Aprendizaje esperado: establece criterios para clasificar materiales cotidianos en mezclas, compuestos y elementos considerando su composición y pureza.
Énfasis: reconocer y clasificar materiales conocidos en el entorno, como mezclas, compuestos y elementos, considerando su composición
¿Qué vamos a aprender?
Lee la siguiente frase célebre del filósofo y psicólogo estadounidense William James.
“Cada forma de clasificar una cosa es solamente una manera de manejarla para un cierto propósito particular”.
NOTA para el docente. Revisa la siguiente propuesta para crear un trabajo colaborativo entre profesoras y profesores.
Se te recomienda la plataforma digital padlet, que ofrece la posibilidad de construir espacios para presentar recursos multimedia; ya sea video, audio, fotos o documentos. Estas herramientas se agregan como notas adhesivas tipo “post-its”.
Con este mural o póster interactivo, podrás publicar, almacenar o compartir recursos de manera individual o en colaboración con tus alumnos y profesores. La plataforma es de uso gratuito, lo único que necesitarás es crear una cuenta. Se puede acceder desde cualquier navegador web en dispositivos móviles:
Reúne objetos de diferentes usos. Por ejemplo: llaves, papel aluminio, azúcar, sal de mesa, agua, refrescos o bebidas de sabor, monedas, enseres de la cocina entre otros.
Si en casa tienes algún tubo de PVC, cobre, aluminio o cualquier otro material, como láminas, clavos, tornillos o herramientas que puedas conseguir sin necesidad de trasladarte, reúne algunos.
También necesitarás tu cuaderno de notas, tu libro de texto de Ciencias. Química, lápiz, bolígrafo y colores.
¿Qué hacemos?
Lee el siguiente ejemplo:
Hace algunos años, en vacaciones, tuve la oportunidad de ir a la playa con mi familia y disfrutar de la belleza del paisaje y del clima. Mi hija y yo estábamos sentados en la arena contemplando el vaivén de las olas cuando mi hija me preguntó ¿por qué al agua de mar se le considera como una mezcla y no como un compuesto si la fórmula del agua es H2O?
Le dije que era una mezcla porque en ella están disueltas muchísimas sustancias. Ella se asombró al saber que, entre esas sustancias, hay una gran cantidad de sales minerales que se obtienen cuando el agua se evapora, pero lo que más le sorprendió, fue que una de ellas es una sal que se llama cloruro de sodio NaCl y se emplea en muchas cosas, por ejemplo, para sazonar y resaltar el sabor de la comida.
Le comenté que a este tipo de sustancia se le conoce como compuesto, ya que está formada por dos elementos: el sodio y el cloro. El sodio es un metal brillante que reacciona violentamente con el aire y el agua, mientras que el cloro es un gas “amarillo” muy venenoso.
Entonces, si esas propiedades presentan los elementos que forman la sal de mesa, ¿cómo es posible que no te envenenes al consumirla en los platillos?
En tus cursos anteriores de Ciencias estudiaste lo importante que es clasificar en Biología y en Física. En esta sesión, reconocerás la importancia de la clasificación en la Química.
Recuerda que todo lo que te rodea es materia “que ocupa un lugar en el espacio y tiene masa”. La materia está compuesta por átomos y que estos forman los diversos materiales de su entorno.
Para comprender de forma práctica estos contenidos llevarás a cabo una actividad de clasificación.
Por ejemplo, clasifica las cosas que tienes en tu lapicera, vacía el contenido sobre tu mesa para trabajar.
Expresa tus ideas y establece criterios, así como las categorías que se te ocurran y que consideres necesarias para clasificarlos.
Puedes hacer lo mismo al guardar tu ropa, con el maquillaje u otros objetos que tengas en casa.
Pero piensa ¿qué criterios utilizarías para clasificar el contenido de tu lapicera?
Por ejemplo, puedes clasificarlos por colores o por tamaños, también por su utilidad y el material con los que están elaborados.
Por ejemplo, los clips y las grapas están hechos de metal; las gomas están hechas de caucho –que es un polímero- y los lápices contienen grafito –que es una forma alotrópica del carbono-.
Aquí es donde puedes aplicar tus conocimientos acerca de la materia y sus propiedades, así como tus habilidades químicas para reconocer de qué están hechos los materiales.
Como habrás notado, en la actividad de clasificación se pueden ordenar de manera diversa todos los objetos escolares.
Los seres humanos, en su afán de conocer y entender lo que les rodea, han intentado clasificar la materia de diferentes formas, pero piensa ¿tu cómo lo harías?
Responde las siguientes preguntas.
- ¿Cómo puedes clasificar los diversos materiales?
- Además del estado de agregación, ¿qué diferencias hay entre ellos?
- ¿El nombre de los materiales te ayudaría a clasificarlos? ¿De qué manera?
- ¿Cuáles de ellos se pueden clasificar como mezclas?
- ¿Cuáles se pueden clasificar como compuestos?
- ¿Cuáles como elementos?
- ¿Cuál es el criterio que permite diferenciarlos?
Podrás comprobar tus repuestas a lo largo de la sesión mediante el desarrollo de las actividades propuestas.
Clasificar sirve para organizar y para ordenar. En tu vida diaria clasificas y agrupas diferentes objetos, plantas o animales, aún sin ponerle ese nombre a tu forma de proceder. El orden que obtienes al agrupar lo que quieres conocer o las cosas que tienes, hace que resulte más fácil la tarea.
La clasificación es una actividad esencial para disciplinas y tareas que lleva a cabo el ser humano. El acto de clasificar es aquel que permite distinguir componentes y agruparlos según sus propiedades. Se aplica en la rutina diaria de cualquier persona, así como para ámbitos académicos y profesionales.
Revisa otro ejemplo:
Cuando regresamos de hacer las compras de la despensa, yo la clasifico separando primero los productos de limpieza, como son los detergentes, limpia vidrios, suavizantes y limpiadores de pisos. Los guardo en el patio para evitar accidentes. Los separo de productos alimenticios como las sopas, galletas y sobrecitos de gelatina, para evitar que se contaminen o impregnen del olor de los detergentes. En la parte de arriba de la alacena acomodo los cereales, en medio todos los productos enlatados y bolsas de azúcar, arroz y frijol; y en la parte de abajo todas las bebidas, pañuelos desechables, papel de baño y otros productos que no sean de primera necesidad.
En química es importante clasificar, ya que permite saber de qué están formadas las sustancias, cómo reaccionan frente a otras sustancias o se comportan en diversas condiciones. También permite saber por qué ocurren ciertos cambios en los materiales.
Es importante recalcar que la materia se presenta en tres estados o formas de agregación: sólido, líquido y gaseoso.
En la naturaleza, sólo algunas sustancias pueden hallarse de modo natural en los tres estados; como es el caso del agua. La mayoría de las sustancias se presentan en un estado concreto.
La teoría cinética permite explicar por qué las sustancias se pueden encontrar en tres estados de agregación: sólido, líquido y gaseoso. El estado en que se encuentre una sustancia depende de la intensidad de las fuerzas de unión o cohesión entre las partículas que la conforman. Además, las propiedades que presenta la materia dependen de su estado de agregación.
Estado sólido:
Los sólidos se caracterizan por tener forma y volumen constantes. Esto se debe a que las partículas que los forman están muy próximas y en posiciones casi fijas, ya que están unidas por fuerzas de cohesión muy intensas.
Las partículas en el estado sólido se disponen de forma ordenada, con una regularidad espacial geométrica.
Estado líquido:
Los líquidos tienen volumen constante al igual que los sólidos. En los líquidos las partículas están unidas por unas fuerzas de cohesión menos intensas que en los sólidos. Sus posiciones no son fijas, por lo que las partículas fluyen libremente y se trasladan con libertad.
Por esta razón los líquidos no tienen forma definida, adoptan la forma del recipiente que los contiene y tienen ciertas propiedades como la fluidez o la viscosidad.
Estado gaseoso:
Los gases, igual que los líquidos, no tienen forma fija; a diferencia de éstos, su volumen tampoco es fijo. En los gases, las fuerzas de cohesión que mantienen unidas las partículas son muy débiles. Las partículas se encuentran muy separadas (el número de partículas por unidad de volumen es muy pequeño).
Después de haber recordado los estados de agregación de la materia, realiza la siguiente actividad.
Observa con atención las siguientes imágenes y clasifica cada ejemplo en el estado de agregación que corresponda. Para ello divide tu hoja en tres columnas y escribe en ellas los estados de agregación, sólido, líquido y gaseoso.

Ahora verifica tus respuestas.

En la columna de los sólidos encuentras a las galletas, el martillo y el hielo.
Ahora en los líquidos: tienes la leche, la miel y el agua.
Por último, los de estado gaseoso: el helio contenido en el globo, el vapor de agua y el dióxido de CO2.
Si es necesario realiza las correcciones pertinentes.
Retomarás otras propiedades físicas de la materia, que te permitirán conocer diferentes formas de agrupar a los materiales.
La conductividad térmica y eléctrica son propiedades importantes de los minerales y otros materiales que se utilizan en la ingeniería de innumerables tecnologías y herramientas. Seleccionar un material con el valor de conductividad adecuado puede aumentar la eficiencia del producto, ahorrar energía y dinero.
Conductividad térmica:
La conductividad térmica de un material o elemento, es una propiedad que ayuda en el desarrollo de tecnologías eficaces de calefacción/enfriamiento.
Revisa algunos ejemplos de conductividad térmica de mayor a menor:
Diamante
Plata
Cobre
Oro
Aluminio
Agua
Madera
Fibra de vidrio
Corcho
Aire
Los materiales con altas conductividades térmicas son cruciales en la ingeniería y el desarrollo de innumerables dispositivos electrónicos de transferencia de calor.
Conductividad eléctrica:
La conductividad eléctrica es la capacidad que tiene una sustancia o material para permitir el paso de corriente eléctrica a través de sí. Es decir, de transportar electrones.
Los materiales sólidos capaces de llevar a cabo la conductividad eléctrica forman una nube de electrones libres que al ser sometidos a un campo eléctrico generan corriente.
Los principales conductores eléctricos son los metales:
Plata
Cobre: Es uno de los elementos mejor conductores y uno de los más usados debido a que su costo es asumible.
Oro
Cuando se trata de conductividad térmica y eléctrica, resulta imprescindible hablar de los materiales dieléctricos o aislantes. Son materiales que ofrecen resistencia al paso de energía térmica o eléctrica. Sirven en la prevención de cortocircuitos y conducción riesgosa de la electricidad.
La forma de clasificar las sustancias es práctica e interesante.
Algunas formas comunes de clasificación de los materiales se relacionan con sus propiedades físicas.
A continuación, revisarás otra manera de clasificar los materiales.
Observa el siguiente video que te ayudará a ir vislumbrando las maneras de clasificar a los materiales. Obsérvalo del minuto 04:12 a 04:52 y del 10:42 a 11:19.
- ¿Mezclas o compuestos?
¿Identificaste algunos conceptos importantes?
Realiza el siguiente organizador grafico que construirás; ya que describirá las diferencias que hay entre elementos, compuestos y mezclas que es como se clasifican los materiales en química.
Recuerda que es muy importante realizar las actividades que se te plantean.
Elementos: son sustancias formadas por los mismos átomos, es decir, mismo número de protones.
No pueden descomponerse en sustancias más simples por métodos físicos ni químicos.
Ejemplos:
Oro (Au), como el que se encuentra en un anillo.
Plata (Ag), como la que se encuentra en una Pulsera de Taxco.
Aluminio (Al), como el que se encuentra en el papel para envolver.
Además del mercurio (Hg) que contienen los termómetros, el oxígeno (O) del aire, el potasio (K), el sodio (Na), el hierro (Fe), el fósforo (P), el calcio (Ca), el yodo (I), el zinc (Zn), por mencionar algunos.
Compuesto: está formado de dos o más elementos que al unirse cambian sus propiedades químicas.
Se unen en proporciones fijas. Es decir, la fórmula del agua es (H2O) formada por 2 átomos de hidrógeno y un átomo de oxígeno, si se aumentara otro oxigeno se le llamaría agua oxigenada o peróxido de hidrógeno (H2O2) formada por 2 átomos de hidrógeno y dos átomos de oxígeno, es decir, se forma otro compuesto con propiedades distintas.
Se pueden separar por procesos químicos como la electrólisis.
Algunos ejemplos son:
Cloruro de sodio (NaCl) formado por una proporción 1:1 de ambos elementos, en una red iónica cristalina.
Monóxido de carbono CO, formado por 1 átomo de carbono y 1 átomo de oxígeno; resulta de la quema de combustibles fósiles y al subir a la atmósfera. Interacciona químicamente con otro oxígeno para producir dióxido de carbono CO2, formado por 1 átomo de carbono y 2 átomos de oxígeno, que tiene propiedades distintas a las del monóxido de carbono CO.
Alcohol metílico, C2 H5OH constituido por 2 átomos de carbono, 6 átomos de hidrógeno y 1 átomo de oxígeno.
El metano CH4 (gas de los pantanos) formado por el átomo carbono y 4 átomos de hidrógeno.
Las mezclas son el resultado de la unión física de dos o más sustancias a las cuales se les llama componentes. Éstos pueden ser elementos o compuestos, y al efectuarse dichas mezclas conservan sus propiedades individuales.
Se unen en proporciones variables, por ejemplo, al preparar un café, le agregas dos cucharadas de azúcar por una de café. Al preparar agua de limón ¿qué cantidades utilizas?, ¿cuántas cucharadas de azúcar mezclas en un litro de agua?
Se separan por procesos o métodos físicos sencillos, por ejemplo, la filtración al preparar café de grano, para que las partículas de mayor tamaño no pueden pasar los filtros.
Las mezclas se pueden clasificar en homogéneas y heterogéneas.
Mezclas homogéneas: son aquellas cuyos componentes forman una sola fase y no se puede distinguir un componente de otro.
Ejemplos de mezclas son:
Las disoluciones. Se caracterizan por su transparencia; ejemplos de esto son el agua con sal, agua con azúcar, agua con alcohol.
Coloides. Se caracterizan por ser translucidos. El tamaño de sus partículas es mayor a las de las disoluciones y presentan el fenómeno Tyndall, como la gelatina, gel antibacterial, niebla, cuando entra la luz solar en una habitación con polvo, aceite de oliva, entre otros.
Suspensiones. Estas se caracterizan por ser opacas, ya que sus partículas son mayores a la de las disoluciones y coloides y se pueden observar a simple vista. Ejemplo, yogurt para beber, agua de horchata, jugo de naranja y smog.
Mezclas heterogéneas: son aquellas cuyos componentes forman 2 o más fases, por lo que se distinguen a simple vista.
Ejemplos: agua con arena, ensalada, aceite y vinagre.
En el organizador grafico que has construido, podrás observar la clasificación de los materiales según su composición, así que es momento de poner a prueba tus conocimientos, y para ello, realiza la siguiente actividad.
Al inicio de la actividad se te pidió recopilar algunos objetos de uso cotidiano.
Debes realizar una tabla con cuatro columnas como la que se muestra en la siguiente imagen. Clasifica tus objetos. Puedes invitar a tus familiares para que juntos aprendan otra forma de clasificar los materiales.
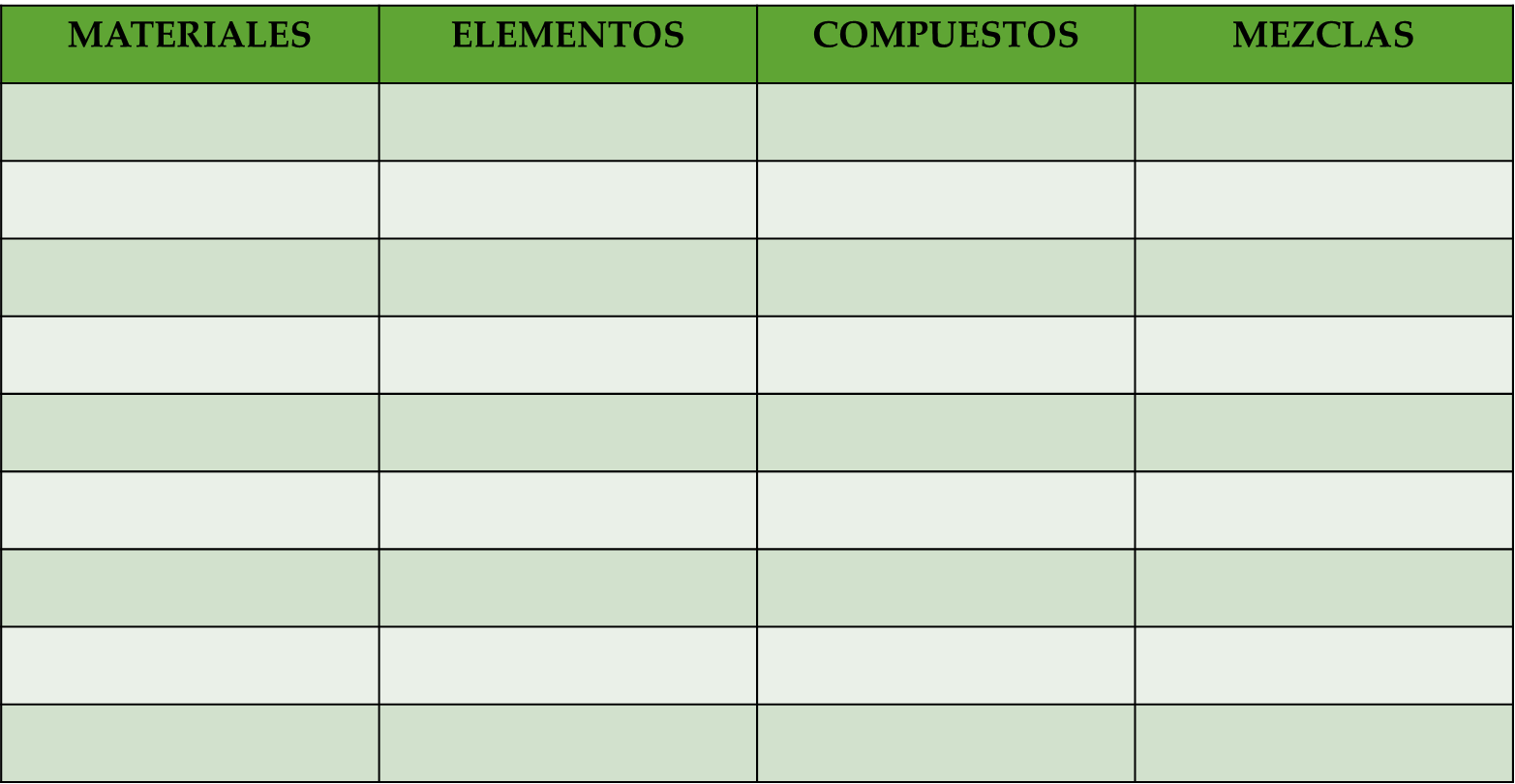
Utilizarás en tu tabla una señalización para marcar la clasificación que corresponda, como, por ejemplo, una palomita.
El primer ejemplo es el oro, cuyo símbolo es Au, contenido en un anillo, su clasificación corresponde a elementos.
Continua con el agua, cuya fórmula química es H2O y es un compuesto.
El gel antibacterial es una mezcla homogénea, sus componentes como carbopol, glicerina, trietanolamina y alcohol, no se pueden distinguir a simple vista.
Un clavo está hecho de hierro cuyo símbolo es Fe, por lo tanto, puedes decir que es un elemento, por su composición de átomos de hierro.
Las monedas mexicanas contienen aleaciones de varios metales como cobre, níquel y zinc. Es decir, son una mezcla homogénea.
El agua con aceite, es posible identificar los componentes a simple vista, por lo que puedes decir que se trata de una mezcla heterogénea.
Cloruro de sodio –cuya fórmula química es NaCl– es un compuesto de cloro y sodio.
El cobre Cu que compone estos tubos es un elemento químico.
Finalmente, la sacarosa C12 H22 O11 es un compuesto químico formado por carbono, hidrógeno y oxígeno.

Has clasificado solo algunos de los muchos materiales que tienes en tu entorno. Sin embargo, ya tienes los conocimientos y habilidades para clasificar los materiales del mundo que te rodea.
Recuerda comparar tus resultados con los de tus compañeros y compartir tus actividades con tus profesoras y profesores.
¿Sabías que? El gas etileno es un compuesto químico orgánico formado por dos átomos de carbono y cuatro átomos de hidrógeno (C2 H4). Es responsable de la maduración y deterioro de algunos vegetales y frutas, principalmente en cítricos.
El oro de 24 quilates (ct) suele ser amarillo, al mezclarlo con otros metales para conseguir oro de 18 ct, o 14 ct, puede cambiar su color. A esta mezcla de metales se le denomina aleación.
¿Por qué es necesario que el oro se mezcle con otros metales?
Existen diversos motivos para hacerlo:
- Conseguir mayor dureza del metal.
- Conseguir variar la gama de colores.
- Reducir costos de producción.
Los metales que pueden mezclarse con el oro son muy variados, cada uno con diferentes propiedades. Depende del resultado que se desea lograr.

Ahora sabes que muchos materiales que utilizas de manera cotidiana tienen diversos componentes, que podrás reconocer e identificar para saber de qué están hechos. También puedes consultar las etiquetas que tienen los productos y saber cuáles son los materiales que lo conforman; aunque no se perciban a simple vista, podrás clasificarlos como mezclas, compuestos o elementos.
El reto de hoy:
Para seguir aprendiendo sobre la clasificación de los materiales se te recomienda los siguientes enlaces de páginas interactivas que contienen modelos y experimentos que te permitirán identificar el tipo de materiales que componen a las sustancias.
http://www.objetos.unam.mx/quimica/sustanciasPuras/
https://www.aev.dfie.ipn.mx/Materia_quimica/temas/tema1/subtema3/subtema3.html#
Se te recomienda también la historia sobre la corona del rey Hierón, en donde aprenderás sobre la densidad y otras curiosidades de los materiales.
¡Buen trabajo!
Gracias por tu esfuerzo.
Para saber más: