¿Cómo se forman y se clasifican las mezclas?
¿Cómo se forman y se clasifican las mezclas?
Aprendizaje esperado: identifica los componentes de las mezclas y las clasifica en homogéneas y heterogéneas.
Énfasis: explicar que las mezclas están formadas de diferentes componentes y que se pueden clasificar en homogéneas y heterogéneas.
¿Qué vamos a aprender?
Lee la siguiente frase del escritor portugués José Saramago, ganador del Premio Nobel de Literatura en 1998.
“La alegría y el dolor no son como el aceite y el agua, sino que coexisten.”
Para esta sesión necesitarás tu cuaderno, tu libro de texto de Ciencias III, lápiz, colores y bolígrafo.
NOTA para el docente. Para esta sesión se te recomienda la siguiente página interactiva:
http://objetos.unam.mx/quimica/sustanciasPuras/index.html
En ella puedes realizar actividades relacionadas con el tema de mezclas.
Por ejemplo, el licuado es muy sencillo de preparar, se colocan en la licuadora alimentos como frutas, leche, miel y luego se licúan y al final obtienes una deliciosa mezcla.
¿Qué sabes de las mezclas?
¿Cómo puedes diferenciar una mezcla homogénea de una heterogénea?
¿Por qué son útiles en nuestra vida?
Anota las respuestas en tu cuaderno durante la sesión.
¿Qué hacemos?
Los perfumes son mezclas complejas de múltiples componentes, algunos volátiles y otros semivolátiles. Son elaborados con materiales que pueden ser mezclas, como los aceites esenciales u otras sustancias.
Un perfume es el resultado de la mezcla de muchos componentes. Muchos de estos ingredientes se combinan de manera compleja para hacerlo distinto y, además, añadirle algún olor en específico.
Con base en la composición, la materia puede clasificarse en dos categorías: sustancias y mezclas.
Una sustancia es una forma de materia cuya composición es uniforme y constante; por ejemplo, el cloruro de sodio que tiene una composición química única, por lo que no cambia de una muestra a otra. Otro ejemplo es el agua, que está compuesta de hidrógeno y oxígeno.
No obstante, el agua de mar no es una sustancia, ya que las muestras tomadas en distintos lugares seguramente tendrían composiciones diferentes a las de otras.
Un cubo de hielo, al cambiar su estado de agregación sólido al líquido, ¿modifica su composición química?
No cambia su composición, sólo modifica su estado físico. Cuando dos o más sustancias se reúnen, el resultado es una mezcla.
Una mezcla es un material formado por dos o más componentes que conservan sus propiedades químicas. La composición de las mezclas es variable y la cantidad de mezclas que se pueden crear mediante la reunión de sustancias es infinita.
Una parte importante de la química se enfoca en el comportamiento de las sustancias. Sin embargo, las sustancias tienden a mezclarse naturalmente, por lo que es difícil mantenerlas puras.
Analiza los siguientes ejemplos: agua y arena, cloruro de sodio y agua. Sabes que el agua puede ser líquida e incolora, y la arena, granulada, por lo que no se disuelve en el agua.
Al mezclarse la arena con el agua, cada una mantiene sus propiedades; el agua y la arena no reaccionan. Por otro lado, la mezcla de cloruro de sodio y agua es a simple vista incolora y parece igual al agua. ¿Cómo puedes saber si se trata de una mezcla?
Si hierves el agua hasta que se evapore, notarás que quedan residuos blanquecinos al fondo del recipiente. Con esto puedes deducir que el agua incolora en realidad estaba compuesta por dos sustancias distintas, agua y cloruro de sodio.
¿Sabías que? Los platillos musicales, que generan una sensación tan agradable al oído, están hechos de bronce o latón. El porcentaje de los metales empleados para su aleación se mantiene en secreto por los fabricantes, pues aunado al tamaño y grosor de los discos, junto con el método del fabricante, es lo que les da su singular acústica.
Esto les provee un sonido que va del agudo al grave o del oscuro al brillante.
Incluso llegan a tener dentro de su aleación oro (Au), por ser un buen conductor del sonido.
Recuerda que las mezclas se clasifican en homogéneas y heterogéneas.
Para organizar la información se te sugiere anotar en tu cuaderno la siguiente tabla para que la complementes.

No olvides que las mezclas homogéneas están formadas por dos o más componentes que no se distinguen a simple vista, ni siquiera con microscopio. Su apariencia es uniforme, es decir, se observa una sola fase.
En una mezcla se le llama soluto al componente que se encuentra en menor proporción con respecto al otro componente, mientras que al componente que se encuentra en mayor proporción con respecto al soluto, se le llama disolvente.
A la mezcla de soluto disuelto en el disolvente se le conoce como disolución.
Es posible representar una mezcla homogénea, con base en el modelo corpuscular. Este modelo considera que toda la materia está formada por partículas en constante movimiento, entre las cuales existe espacio vacío.
Con base en los colores del CPK, analiza los siguientes ejemplos: el átomo de oro está representado por esferas de color verde, la molécula de hidrógeno está representada por dos esferas unidas de color blanco, el compuesto metano por esferas de color gris y blanco, y la mezcla, que está representada por todos los anteriores.
Las moléculas del agua están formadas por dos átomos de hidrógeno y uno de oxígeno, representados por esferas de color blanco y rojo, respectivamente.
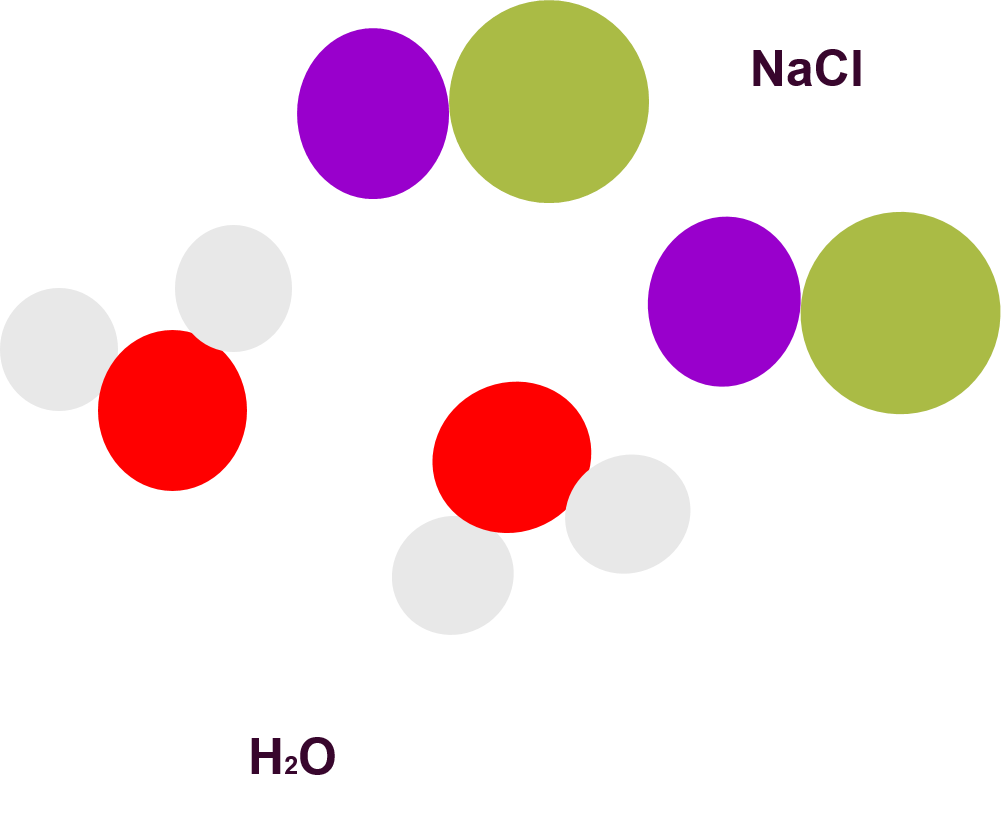
El cloruro de sodio está formado por sodio y cloro, representado por esferas de color morado y verde respectivamente. La imagen representa una mezcla homogénea o disolución. Observa los dos componentes: cloruro de sodio y agua distribuidos uniformemente.
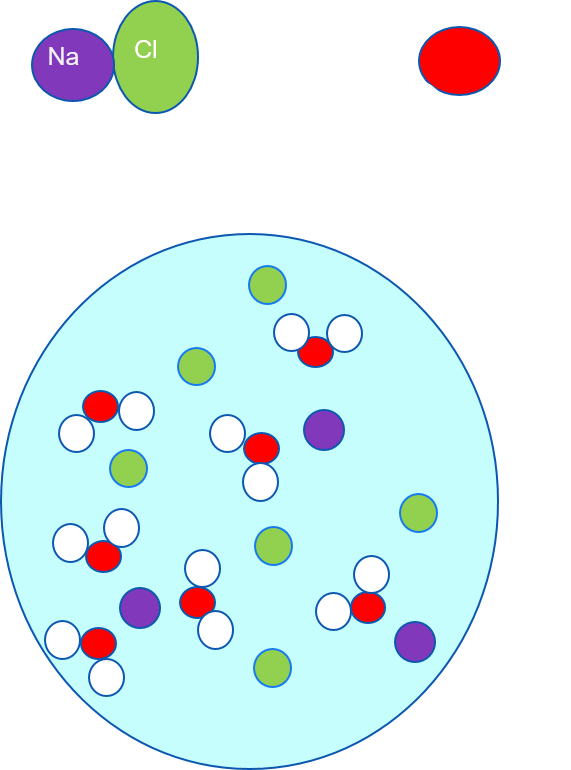
Como el cloruro de sodio (NaCl) está en disolución acuosa, se separa formando iones de sodio (Na+) y cloruro (Cl–) que observas disueltos entre las moléculas de agua.

Las aleaciones son una mezcla de distintos componentes, principalmente de metales.
Observa el modelo corpuscular del bronce, el cobre y el estaño que lo conforman están distribuidos uniformemente. Las esferas de color gris representan el estaño (Sn), las esferas de color dorado representan los átomos de cobre (Cu). Al encontrarse en estado sólido, observas que todas las esferas están agrupadas ordenadamente porque forman redes cristalinas, como observaste anteriormente.
A las mezclas homogéneas también se les puede llamar disoluciones, ya que son el resultado de reunir un sólido con otro sólido, un líquido con otro líquido, un líquido con un sólido o un gas con otro gas.
Las mezclas que constan de dos o más fases físicamente son distintas, ya que lo que se observa a simple vista son sus fases. A estas mezclas se les conoce como mezclas heterogéneas.
Al componente de la mezcla que está en menor proporción se le llama fase dispersa, y al que se encuentra en mayor proporción, fase dispersante.
Observa el ejemplo. Tienes una mezcla de flores de jamaica que se dejaron reposar en agua toda la noche, ¿qué tipo de mezcla es?
A simple vista puedes decir que es una mezcla heterogénea, pero ¿qué sucede si se retiran las flores de jamaica? Sería una disolución, debido a que se obtuvo un extracto de la jamaica, o agua de jamaica, evidenciado por el color rojo translúcido.
En materiales como el talco, que es un sólido, y el agua, que es un líquido, al mezclarse, se observa que aún se distingue cómo el sólido no se integra al líquido y queda esparcido. Esto es conocido como suspensión.
Otro ejemplo muy común es la penicilina en polvo, a la cual se le tiene que agregar agua hervida, agitar y tomar enseguida, pues de lo contrario la penicilina se asienta en el fondo del vaso y es difícil tomar la sustancia activa.
Por ejemplo, mezcla agua y aceite. Agita. ¿Qué es lo que observas? Se distinguen a simple vista las dos fases. Éstas son las llamadas emulsiones, por lo que se trata de una mezcla heterogénea.
Observa el siguiente modelo corpuscular, en él, los componentes de la mezcla se encuentran en dos fases, unos separados de otros. Se diferencian porque las esferas de color amarillo se encuentran conglomeradas de un solo lado, en la superficie, y las de color azul, abajo.
En la siguiente imagen se observan también 2 fases que representan el aceite y al agua. Por la densidad, el agua está abajo, y el aceite, arriba.

Observa el siguiente modelo corpuscular. En él se representa la suspensión de agua y talco. En la imagen de la izquierda se pueden ver las partículas de talco, representadas por los puntitos azules y suspendidas en el agua al ser observadas de lejos.
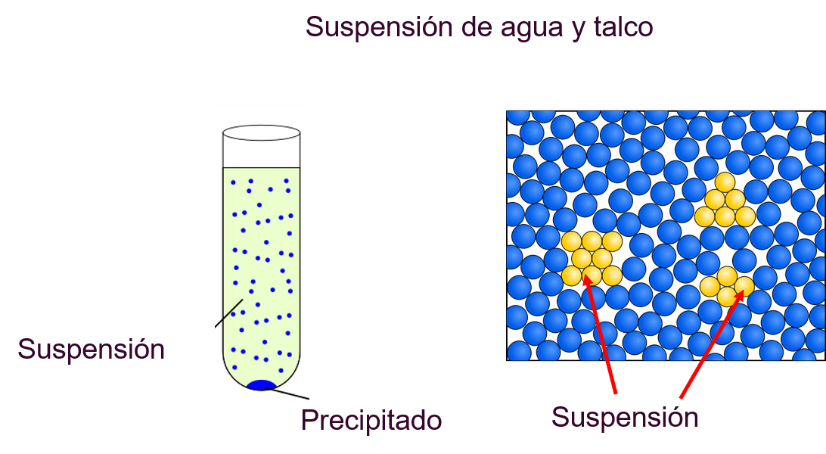
Si haces un acercamiento, podrías observar algo como en la imagen del lado derecho. La fase dispersa, que en este caso es el talco, representada con las esferas amarillas, no se distribuye en la fase dispersante, o sea, en el agua, y forma agregados, por lo que no hay una distribución uniforme.
Otro ejemplo es el jugo de naranja sin colar, una combinación del agua que contiene la fruta más la pulpa, el bagazo y hasta unas semillas. ¿Qué tipo de mezcla es? ¿Y si se cuela el jugo de naranja?
Anota tus respuestas.
En el suelo se multiplican miles de formas de vida. La mayoría, invisibles para nuestros ojos. Una hectárea de tierra fértil puede contener más de 300 millones de pequeños invertebrados, insectos, arañas, lombrices y otros animales diminutos.
El suelo que cabe en una cucharada puede contener un millón de bacterias, así como cientos de miles de células de levaduras y pequeños hongos.
Las lombrices, bacterias y hongos producen una forma estable de materia orgánica.
Todos crean las condiciones para que las plantas respiren, absorban agua y nutrimentos, desarrollen sus raíces y se pueda disponer de ellas.
Continúa experimentando. Por ejemplo, el gel antibacterial, sanitizante y desinfectante de verduras.
Sabes que el gel es útil para ser utilizado como antibacterial, ya que es una mezcla de agua con alcohol a 70%, pero ¿qué contiene el sanitizante?
Entre los más comunes, se encuentran los que contienen amonio cuaternario, otro es de extracto de semillas.
En ocasiones es difícil distinguir una mezcla homogénea de una heterogénea porque el tamaño de partícula es muy pequeño, a simple vista no se puede ver y se podría decir que está en la frontera entre una mezcla homogénea y heterogénea.
A este tipo de mezcla se le conoce como soles o coloides. Existe una prueba que lleva el nombre de quien la descubrió: la prueba Tyndall.
Esta prueba consiste en hacer pasar un haz de luz en la mezcla, si observas la línea que atraviesa al líquido, podrás decir con seguridad que es un coloide, es decir, una mezcla heterogénea.
Esto se debe a que la luz, que es un flujo de electrones, interactúa con las partículas suspendidas de la fase dispersa y por eso puedes observar el haz de luz.
Si no lo observas, quiere decir que se trata de una disolución y, por lo tanto, es una mezcla homogénea.
Se pasa por el extracto de semillas. ¿Qué observas? Si no se observa ningún rayo, entonces es una mezcla homogénea.
Si se realiza lo mismo con el sanitizante, no se observa ningún rayo de luz; también es una mezcla homogénea.
Ahora con el gel, se observan burbujas de aire de color pardo. Se puede observar un haz de luz por lo tanto es una mezcla heterogénea o coloide.
Por último, se tienen dos bebidas, ambas son de manzana, pero una es traslúcida y la otra es opaca.
¿Cuál es la mezcla homogénea y cuál la heterogénea?
El néctar que contiene pulpa y es opaco es la mezcla heterogénea, y el que está traslúcido es la mezcla homogénea.
¿Te has preguntado qué sentido tiene aprender sobre las mezclas y sus diferentes tipos?
Si observas a tu alrededor, podrás notar que todo o casi todo está compuesto por mezclas. En la naturaleza es muy difícil encontrar sustancias puras. Inclusive el aire que respiras todos los días es una mezcla de distintos gases; el aire seco contiene aproximadamente 78% de nitrógeno, 21% de oxígeno y 1% de otros gases como el dióxido de carbono, neón, helio, kriptón, metano, xenón y ozono.
Además de los componentes anteriores, el aire húmedo contiene vapor de agua, que varía de 1% a 4% según la latitud y el clima.
Anota en tu cuaderno: ¿qué criterios utilizarías para clasificar mezclas en homogéneas y heterogéneas?
Realiza un organizador gráfico, que puede ser un mapa mental. Recuerda que éste debe ir con dibujos e ilustraciones.
Durante esta sesión aprendiste sobre la composición de una mezcla, y que los componentes conservan sus propiedades químicas.
Asimismo, identificaste cómo se clasifican en mezclas homogéneas y heterogéneas.
Comprendiste que las mezclas están formadas por dos o más componentes y que las mezclas homogéneas también se conocen como disoluciones, en las cuales es posible que se mezclen sólidos, gases o líquidos; un líquido y un gas, o un sólido y un líquido. Y que consta de una sola fase, donde al componente en menor proporción se le llama soluto y al componente en mayor proporción se le llama disolvente.
Las mezclas heterogéneas están formadas por dos o más componentes donde se observan al menos dos fases: la que se encuentra en menor proporción es llamada fase dispersa y la que se encuentra en mayor proporción se llama fase dispersante.
Con base en el tamaño de la partícula, se llaman suspensiones, que son las de mayor tamaño; le siguen las emulsiones, y las de partícula más pequeña son llamadas coloides.
Por medio del efecto Tyndall puedes diferenciar una mezcla homogénea de una heterogénea llamada coloide.
Las palabras clave en esta sesión fueron:
- Mezclas
- Mezclas homogéneas
- Mezclas heterogéneas
- Disolución
- Soluto
- Disolvente
- Coloides
- Emulsión
- Suspensión
- Efecto Tyndall
El reto de hoy:
Para seguir aprendiendo, se te recomienda la lectura del libro:
¡Es elemental!, del autor Winston, Robert, de la serie Espejo de Urania.
Este libro te introduce de forma sencilla al mundo de la química. Mira a tu alrededor y descubre cómo la química está en todas partes.
También puedes leerlo en la siguiente dirección electrónica:
https://feoruiz.files.wordpress.com/2019/09/es-elemental-pag-1-62.pdf
¡Buen trabajo!
Gracias por tu esfuerzo.