Solubilidad y el agua
Solubilidad y el agua
Aprendizaje esperado: identifica al agua como disolvente de varios materiales a partir de su aprovechamiento en diversas situaciones cotidianas.
Énfasis: 1/4 experimentar con diferentes materiales para clasificarlos en solubles en agua.
¿Qué vamos a aprender?
Aprenderás a identificar al agua como disolvente de varios materiales a partir de su aprovechamiento en diversas situaciones cotidianas. Seguirás aprendiendo acerca de los materiales que nos rodean.
¿Qué hacemos?
En sesiones pasadas has visto cosas muy interesantes, como: Los diferentes tipos de materiales y los usos que les damos según sus características.
Los estados físicos en los que se encuentran la mayoría de los materiales que utilizas, las características de tres estados: sólido, líquido y gaseoso, aunque al final nos mencionaste un cuarto estado; el plasma.
Es importante que tengas claras las características de los tres estados más comunes, para que puedas observarlos y reconocerlos en nuestro entorno y entender los temas que veras en las siguientes sesiones. Me parece que identificar los tres estados físicos y sus características es algo que debes recordar.
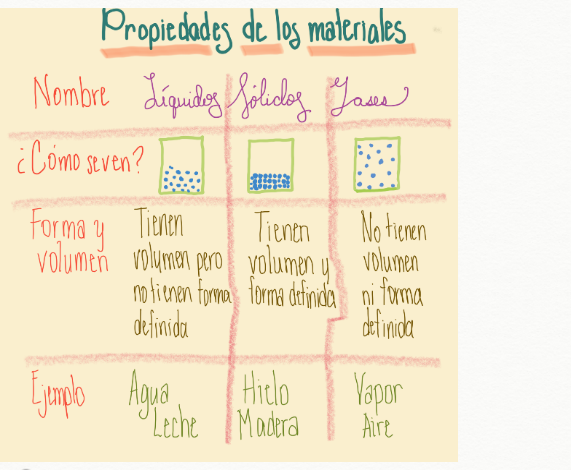
Es importante recordar:
– El nombre de cada estado.
– La característica relacionada con la forma y volumen de cada uno.
– También, podemos poner los dibujos que observamos con los “Lentes particulares” porque hay diferencias entre los tres estados físicos.
– Por último, pondría uno o dos ejemplos de cada estado para recordarlos, y con ellos comparar otros materiales.
¿Recuerdas el nombre de los tres estados?
Seguiremos hablando de los materiales y sus estados. Por ejemplo, ¿Tú sabías que los materiales que se encuentran en un estado pueden relacionarse con los que se encuentran en otros estados?

Es sesiones posteriores te darás cuenta que pueden cambiar en diferentes estados o se combinan a esto se le llama solubilidad.

Solubilidad: Es la capacidad de un material de mezclarse uniformemente con otro, es decir, que se disuelve en él. Ve a qué se refiere con que un material se disuelve en otro.

Soluto: Es cualquier sustancia líquida, sólida o gaseosa que se puede disolver.
Solvente: Es cualquier sustancia en la que se puede disolver algo. También puede llamarse disolvente.
Siempre que se habla de solubilidad debes considerar a estos dos personajes, los solutos, que es lo que se “deshace” y el solvente, que es lo que provoca que se “deshaga”.
No puede haber uno sin el otro.
Si yo digo solubilidad, ¿A qué te suena? lo primero que se te viene a la mente es el café s-o-l-u-b-l-e. Observa cómo se comporta el café.
¿Qué estados físicos identificas? El café es sólido y el agua es líquido, el café se deshizo y pinto toda el agua de color café muy obscuro.
Recuerda que el soluto es cualquier sustancia líquida, sólida o gaseosa que se deshace o disuelve, mientras que, el solvente es cualquier sustancia en la que se puede deshacer o disuelve algo.
¿Qué se disolvió?
El café se deshizo o disolvió en el agua por lo tanto el café es el soluto. Fue el agua la que lo deshizo, por lo tanto, el agua es el solvente, entonces puedes identificar que hay materiales que actúan como solutos y materiales que lo hacen como solventes.
Antes de terminar, te invito a descubrir un dato interesante:


El Premio Nobel es un galardón internacional que cada año otorga la Fundación Nobel, en Estocolmo, Suecia, a personas que hayan hecho investigaciones sobresalientes, inventado técnicas o equipamiento revolucionario o hayan hecho contribuciones notables a la sociedad. El premio se instituyó como la última voluntad de Alfred Nobel, industrial sueco que inventó la dinamita, el 27 de noviembre de 1895.
Los investigadores Paul Crutzen, Mario Molina y Sherwood Rowland fueron galardonados en 1995 con el Premio Nobel de Química. Su trabajo demostró, entre otros aspectos, que los gases utilizados en la refrigeración y los aerosoles destruyen la capa de ozono.
Si te es posible consulta otros libros y comenta el tema de hoy con tu familia.
¡Buen trabajo!
Gracias por tu esfuerzo.
Para saber más:
Lectura
